PAXLOVID – Terobosan Tepat Waktu Antivirus COVID-19
Alhamdulillah, pada 22 Desember 2021, FDA telah memberikan otorisasi untuk penggunaan darurat (Emergency Use Authrorization/EUA) Paxlovid dalam pengobatan COVID-19. Kita sangat menantikan berita baik ini yang bertepatan dengan meningkatnya gelombang kedua dan ketiga karena varian Delta di beberapa negara dan munculnya varian baru Omicron yang dinyatakan sebagai Varian of Concern (VOC) oleh WHO pada 26 November 2021.
Perlu kita tilik lagi ke belakang, bahwasanya wabah SARS-CoV-2 pada 2019 telah mengakibatkan 279 juta kasus terkonfirmasi COVID-19 dan menyebabkan >5,3 juta kematian secara global per Desember 2021 (WHO, 2021). SARS-CoV-2 adalah RNA-coronavirus yang sangat menular dan dapat menyebabkan kasus serius seperti pneumonia serta gejala long Covid. Meskipun vaksin COVID-19 telah dikembangkan dan terbukti dapat menurunkan prevelensi dan kesakitan pada pasien COVID-19, sebagian besar orang tidak dapat mendapatkannya karena kondisi medis yang sudah ada sebelumnya atau tidak mau divaksinasi. Selain itu, adanya hambatan akses global seperti di Negara Dunia Ketiga.
Terapi oral khusus untuk SARS-CoV-2 sangat dibutuhkan untuk mencegah rawat inap, mencegah kesakitan, dan kematian. Penggunaan kembali obat-obatan (repurposing drug) sebagai agen antivirus SARS-CoV-2 sejauh ini kurang efektif dan pemberiannya secara per intra vena juga kurang menyenangkan. Pendekatan terbaru dalam penemuan obat antivirus COVID-19 yang cukup potensial adalah dengan menghambat suatu protease utama (main protease) yang terlibat dalam pemecahan poliprotein yang terlibat dalam replikasi virus. Obat PF-07321332 (Paxlovid) dapat diberikan secara oral, memiliki selektivitas dan profil keamanan yang baik. Paxlovid 90% efektif mencegah rawat inap dan kematian pasien berisiko tinggi. Selain itu, paxlovid juga mampu melawan VOC Sars Cov-2, termasuk Omicron. Paxlovid juga dilaporkan dapat menghambat coronavirus lainnya, termasuk SARS dan MERS.
Berbagai negara sepertinya akan segera menggunakan Paxlovid. AS dilaporkan telah mengamankan 10 juta dosis Paxlovid. Lalu, Korea Selatan menjadi negara Asia pertama yang telah menyetujui penggunaan Paxlovid. Sementara itu, negara di Eropa masih belum menyetujui penggunaan Paxlovid. Indonesia sendiri dilaporkan masih menunggu kajian efikasi, khasiat, dan efek samping dari paxlovid yang dilakukan oleh BPOM.
Bagaimana mekanisme kerja Paxlovid?
Paxlovid bukanlah suatu repurposing drug melainkan memang obat yang disintesis dan didesain khusus untuk Sars Cov-2. Paxlovid merupakan kombinasi antara obat antivirus bernama Nirmatrelvir dan Ritonavir. Nirmatrelvir adalah inhibitor kovalen, mengikat langsung ke residu katalitik sistein (Cys145) dari enzim protease (Mpro) seperti yang ditunjukkan pada langkah 3, yang selanjutnya akan menghentikan langkah 4–6 (lihat gambar). Penghambatan Mpro adalah titik strategis, yang membuat virus gagal untuk bereplikasi. Ritonavir berfungsi untuk memperlambat metabolisme nirmatrelvir oleh enzim sitokrom untuk mempertahankan konsentrasi nirmatrelvir tetap tinggi di dalam darah.
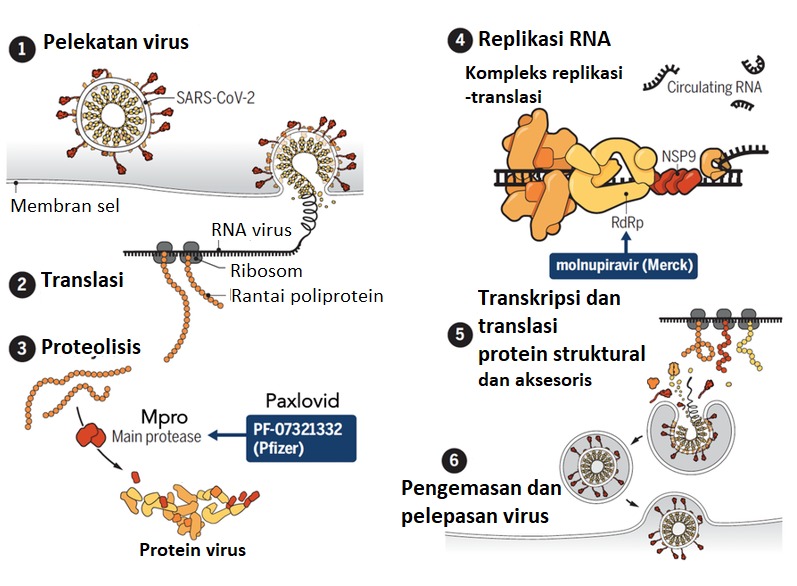
Mekanisme antivirus Paxlovid dan Molnupiravir. (Gambar dimodifikasi dari science.org)
Siapa penerima dan bagaimana penggunaan Paxlovid?
Paxlovid akan tersedia dalam bentuk blister berisi dua tablet Nirmatrelvir 150 mg, dan satu tablet Ritonavir 100 mg. Ritonavir merupakan obat untuk HIV, tetapi di sini digunakan untuk memperlambat metabolisme nirmatrelvir. Pasien yang juga menerima obat yang dimetabolisme oleh enzim sitokrom perlu penyesuaian dosis, misalnya pada obat golongan statin, pengencer darah, dan antidepresan. Paxlovid dapat diberikan jika pasien:
- Berusia > 12 tahun atau BB 39 kg,
- Dinyatakan positif COVID-19, dan
- Menggunakan resep dokter.
Hal yang perlu diingat, paxlovid bukanlah obat untuk mencegah COVID. Jadi, tidak bisa diberikan sebagai agen preventif.
Lalu, bagaimana dengan Molnupiravir?
Sebelumnya, molnupiravir digadang-gadang sebagai obat pertama anti-COVID-19. Akan tetapi, hasil uji klinis lengkap molnupiravir kurang begitu menggembirakan. Pada awal fase klinis, Merck melaporkan adanya pengurangan relatif (efektivitas obat) 50% dan manfaat absolut 7 per 100 orang untuk pasien rawat inap. Sementara hasil uji klinis menyatakan pengurangan hanya ~30% relatif dan hanya 3 per 100 pengurangan absolut dari pasien rawat inap. Pada 23 Desember 2021 (sehari sesudah EUA Paxlovid), FDA memberikan EUA bagi penggunaan malnopurivir di AS.
FDA mengizinkan pemberian molnupiravir untuk orang dewasa dengan gejala awal COVID-19 yang menghadapi risiko rawat inap tertinggi, termasuk orang tua dan mereka yang memiliki kondisi seperti obesitas dan penyakit jantung. Molnupiravir mungkin efektif digunakan sebagai pengobatan COVID-19 ringan hingga sedang pada orang dewasa tertentu ketika alternatif COVID-19 pilihan pengobatan yang disahkan oleh FDA tidak dapat diakses atau sesuai secara klinis. Beberapa efek samping serius dari obat ini adalah dapat memengaruhi pertumbuhan tulang dan tulang rawan sehingga dikontraindikasikan pada pasien di bawah 18 tahun. Selain itu, uji pre-klinis pada hewan menunjukkan adanya bukti teratogenik sehingga obat ini juga dikontraindikasikan pada wanita hamil. Molnupiravir diberikan sebagai empat kapsul 200 miligram yang diminum setiap 12 jam selama lima hari, dengan total 40 kapsul. Molnupiravir tidak diizinkan untuk digunakan lebih dari lima hari berturut-turut.
Mencegah lebih baik daripada mengobati
Adanya Paxlovid/ Molnupiravir seharusnya tidak mengurangi pemberian vaksinasi dan juga penerimaan booster vaksin. Yang perlu digaribawahi adalah Paxlovid atau Molnupiravir bukanlah untuk pencegahan primer, tidak seperti vaksinasi. Kegiatan pencegahan Covid-19 seperti 3 M (memakai masker, menjaga jarak, mencuci tangan pakai sabun), 3T (testing, tracing, treatment), dan vaksinasi merupakan langkah yang tepat dalam pengendalian pandemi. Peranan pemerintah sebagai pemangku kebijakan dalam pengendalian pandemi harus tegas dan terus menerus mengingatkan kepada masyarakat. Kita sebagai tenaga kesehatan juga memiliki andil yang besar dalam membantu pemerintah dengan berpartisipasi mengedukasi masyarakat tentang pengendalian dan pencegahan Covid-19.
Terakhir, mari liburan akhir tahun dan tahun baru kita isi dengan hal -hal yang bermanfaat di rumah. Semoga tahun 2022 pandemi segera selesai. Amien.
Ditulis oleh Dr. apt. Asih Triastuti, M. Pharm (Dosen Jurusan Farmasi UII)
Referensi:
WHO Solidarity Trial Consortium. Repurposed Antiviral Drugs for Covid-19 – Interim WHO Solidarity Trial Results. N Engl J Med. 2021 Feb 11;384(6):497-511. doi: 10.1056/NEJMoa2023184. Epub 2020 Dec 2. PMID: 33264556; PMCID: PMC7727327.
Riva L, et al., Discovery of SARS-CoV-2 antiviral drugs through large-scale compound repurposing. Nature. 2020 Oct;586(7827):113-119. doi: 10.1038/s41586-020-2577-1. Epub 2020 Jul 24. PMID: 32707573; PMCID: PMC7603405.
Owen DR, Allerton CMN, Anderson AS, Aschenbrenner L, Avery M, Berritt S, Boras B, Cardin RD, Carlo A, Coffman KJ, Dantonio A, Di L, Eng H, Ferre R, Gajiwala KS, Gibson SA, Greasley SE, Hurst BL, Kadar EP, Kalgutkar AS, Lee JC, Lee J, Liu W, Mason SW, Noell S, Novak JJ, Obach RS, Ogilvie K, Patel NC, Pettersson M, Rai DK, Reese MR, Sammons MF, Sathish JG, Singh RSP, Steppan CM, Stewart AE, Tuttle JB, Updyke L, Verhoest PR, Wei L, Yang Q, Zhu Y. An oral SARS-CoV-2 Mpro inhibitor clinical candidate for the treatment of COVID-19. Science. 2021 Dec 24;374(6575):1586-1593. doi: 10.1126/science.abl4784. Epub 2021 Nov 2. PMID: 34726479.
https://www.science.org/content/article/pfizer-antiviral-slashes-covid-19-hospitalizations
https://erictopol.substack.com/p/why-paxlovid-is-a-just-in-time-breakthrough
https://www.abc.net.au/news/2021-12-24/fda-approves-mercks-molnupiravir-pill/100723836


