MENGATASI KEKHAWATIRAN VAKSIN COVID-19 DENGAN SAINS

Gambar: Ilustrasi dari freepik.com
Sejak COVID-19 dinyatakan sebagai pandemi oleh organisasi kesehatan dunia (WHO) pada 11 Maret 2020, pertanyaan yang diajukan semua orang adalah mengapa butuh waktu lama untuk memproduksi vaksin. Berpacu dengan waktu, para peneliti dan produsen vaksin telah berupaya semaksimal mungkin untuk mengembangkan vaksin COVID-19.
Sepertinya, permulaan dari akhir pandemi ini semakin dekat. Akan tetapi, sekarang kita dihadapkan pada kekhawatiran lain. Pertama, apakah dosis vaksin akan cukup untuk dibagikan bagi semua orang. Kedua, adanya sekelompok orang yang tidak mau divaksinasi karena produksi dan pengembangan vaksin dirasa sangat cepat.
Menurut survei Populi Center yang dirilis pada 9 November 2020, 40,0 persen masyarakat Indonesia tidak bersedia menggunakan vaksin pembagian dari pemerintah. Dalam pertanyaan khusus, masyarakat yang tidak bersedia diberi vaksin mayoritas menjawab takut akan bahaya/risiko kesehatan sebesar 46,5 persen ; tidak percaya vaksin menyembuhkan sebesar 15,2 persen ; dan tidak dapat memastikan vaksin halal sebesar 13,3 persen. Jumlah orang yang menolak vaksinasi atau menundanya akan bertambah kecuali kekhawatiran publik atas kemanjuran dan keamanan vaksin COVID-19 ini ditangani. Jika tidak, hal ini akan menjadi bencana karena akan memungkinkan virus untuk terus beredar sehingga memperpanjang pandemi.
Oleh karena itu, satu-satunya cara untuk meminimalkan penderitaan karena COVID-19 sehingga dapat melanjutkan kehidupan normal, perdagangan, perjalanan/travel, dan pendidikan adalah dengan menghentikan penyebaran virus. Namun, jika untuk mencapai kondisi ini hanya bergantung pada vaksin saja, tentu tidak cukup. Untuk itu, kita membutuhkan sebanyak mungkin orang untuk dilindungi (membentuk herd immunity) di seluruh dunia secara manusiawi dan secepat mungkin.
Mengapa produksi vaksin COVID-19 berlangsung sangat cepat?
Selama berbulan-bulan kita telah berulang kali diberi tahu bahwa biasanya dibutuhkan lebih dari satu dekade untuk mengembangkan vaksin. Oleh karena itu, cukup masuk akal untuk bertanya bagaimana vaksin COVID-19 ini dapat diproduksi dalam waktu kurang dari setahun?
Untuk memahami hal ini, penting untuk diingat bahwa uji klinis hanyalah satu tahap dari proses pengembangan vaksin yang biasanya berlangsung lama (lihat gambar pengembangan vaksin di bawah). Pada tahap pre-klinik (sebelum vaksin diuji kepada manusia), diperlukan waktu bertahun-tahun untuk mengembangkan antigen yang sesuai. Antigen adalah bagian dari vaksin yang digunakan untuk memicu respons imun.
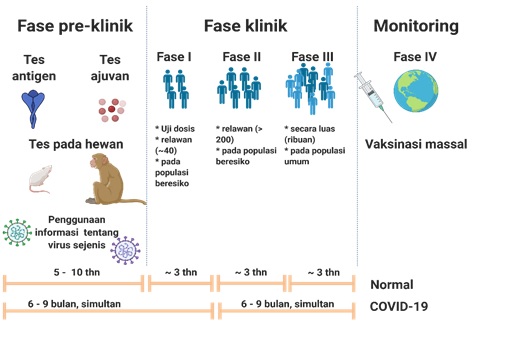
Gambar tahapan pengembangan vaksin
Antigen COVID-19 pertama dipetakan dalam beberapa jam setelah genom virus corona dipublikasikan pada 31 Januari 2020 oleh Institut Pasteur, Prancis. Oleh karena itu, pengembangan vaksin RNA virus sangat cepat. Demikian pula waktu pengembangan vaksin lain yang lebih tradisional dapat dipercepat dengan menggali informasi dari virus terkait seperti antigen virus SARS, Mers, dan virus corona. Proses inilah yang dapat menghemat waktu kita bertahun-tahun.
Alasan penting lain mengapa pengembangan vaksin biasanya memakan waktu lama adalah bahwa produsen vaksin biasanya melakukan uji klinis secara berurutan, lalu berhenti di antara setiap fase, dan kadang-kadang mengulangi uji coba dengan perubahan antigen seperti yang telah dijelaskan. Selain itu, produsen biasanya menunggu sampai calon vaksin mereka lolos uji klinis dan melewati semua peraturan sebelum meningkatkan fasilitas produksi. Dengan demikian, mereka dapat memproduksi vaksin dalam jumlah besar. Mengingat satu pabrik dapat menelan biaya lebih dari setengah miliar dolar (sekitar 7 triliun rupiah) dan kandidat vaksin pada tahap klinis masih memiliki peluang kurang dari 20 persen untuk berhasil, dapat dimengerti mengapa produsen biasanya enggan melakukan investasi yang signifikan sampai mereka yakin bahwa produk tersebut berlisensi dan dapat dipasarkan. Kondisi ini dapat menambah lamanya waktu yang dibutuhkan sebelum vaksin tersedia.
Sementara itu, situasi sangat berbeda pada Covid-19 karena telah menjadi ancaman global. Oleh karena itu, para ilmuwan telah menjawab tantangan tersebut dengan mengembangkan 57 kandidat vaksin yang sedang dalam tahap uji klinis: 40 dalam uji fase I-II dan 17 dalam uji fase II-III yang didukung dengan investasi besar-besaran dari negara-negara maju. Situasi berbeda lainnya adalah karena terdapat kolaborasi global yang melibatkan 189 pemerintahan dan pelaku ekonomi yang mewakili hampir 90 persen dari populasi global melalui ACT accelerator yang diinisiasi oleh negara-negara G20 dan WHO. Kolaborasi ini memastikan akses ke vaksin Covid-19 lebih cepat, adil, dan setara bagi orang-orang di seluruh dunia. Pemerintah dalam hal ini membantu produsen berbagi risiko dan mendorong mereka untuk meningkatkan dan mulai memproduksi vaksin dalam volume besar sebelum vaksin tersebut berlisensi. Hal ini berarti bahwa setelah disetujui oleh otoritas untuk digunakan, pemerintah dapat memulai vaksinasi sehingga dapat menghemat waktu bertahun-tahun.
Sebagai tambahan, pada uji klinis, efisiensi waktu dilakukan dengan melaksanakan berbagai fase hampir secara paralel, bukan satu demi satu. Selain itu, pengadaptasiannya dilakukan seiring berjalannya waktu. Hal ini tidak hanya memungkinkan untuk mempercepat proses, tetapi juga untuk benar-benar membantu menyempurnakan vaksin tersebut. Kemudian, di setiap tahap dapat ditambahkan uji pada kelompok risiko sehingga diperoleh profil yang lebih lengkap tentang seberapa efektif vaksin di berbagai demografi yang berbeda. Sebagai contoh, vaksin Sinovac yang diuji klinik pada fase III di beberapa negara seperti Brazil, Cili, Filipina, Indonesia, dan Turki melibatkan lebih dari 20.000 relawan, tentu saja dengan tetap memperhatikan aspek keselamatan.
Kapan Indonesia akan memulai vaksin COVID-19?
Pada 2 Desember 2020, NHS menyetujui penggunaan vaksin Covid-19 produksi Pfizer-BioNTech di Inggris. Lalu, pada 11 Desember 2020, FDA menyetujui penggunaan darurat vaksin Covid-19 produksi Pfizer tersebut di AS. Sementara itu, pemerintah Indonesia telah memesan sekitar 143 juta dosis vaksin Sinovac dengan total 1,2 juta dosis vaksin masuk ke Tanah Air pekan lalu. Vaksin tersebut kini disimpan di gudang PT Bio Farma di Bandung dan menunggu BPOM untuk memberikan lampu hijau untuk penggunaan darurat vaksin sebelum dapat memulai vaksinasi. Awal Januari, Bio Farma akan menyampaikan laporan sementara yang berisi bukti efikasi, imunogenisitas, dan keamanan (serta kehalalan) vaksin tersebut kepada BPOM untuk membantu memastikan otorisasi penggunaan. Selain itu, pemerintah juga akan memastikan tersedianya fasilitas rantai dingin (cold chain) untuk menjaga stabilitas vaksin dan telah mempersiapkan petugas kesehatan sebagai tenaga vaksinator. Masyarakat Indonesia akan menerima vaksin yang aman dan efektif, sesuai dengan komitmen BPOM dan pemerintah. Sembari menunggu hasil uji klinik vaksin, edukasi dan sosialisasi kepada masyarakat akan vaksin COVID-19 sangat diperlukan.
Ditulis oleh Dr. apt. Asih Triastuti, M. Pharm (Dosen Jurusan Farmasi UII)
Sumber:
https://www.raps.org/news-and-articles/news-articles/2020/3/covid-19-vaccine-tracker
https://ourworldindata.org/covid-vaccinations
https://www.cdc.gov/coronavirus/2019-ncov/vaccines/effectiveness.html
https://www.sciencedaily.com/releases/2020/01/200131114748.htm